RÉPONSE ACR 20 À LA SEMAINE 16 : OTEZLA A PROCURÉ UNE AMÉLIORATION STATISTIQUEMENT SIGNIFICATIVE COMPARATIVEMENT AU PLACEBO (PARAMÈTRE D’ÉVALUATION PRINCIPAL)1,9
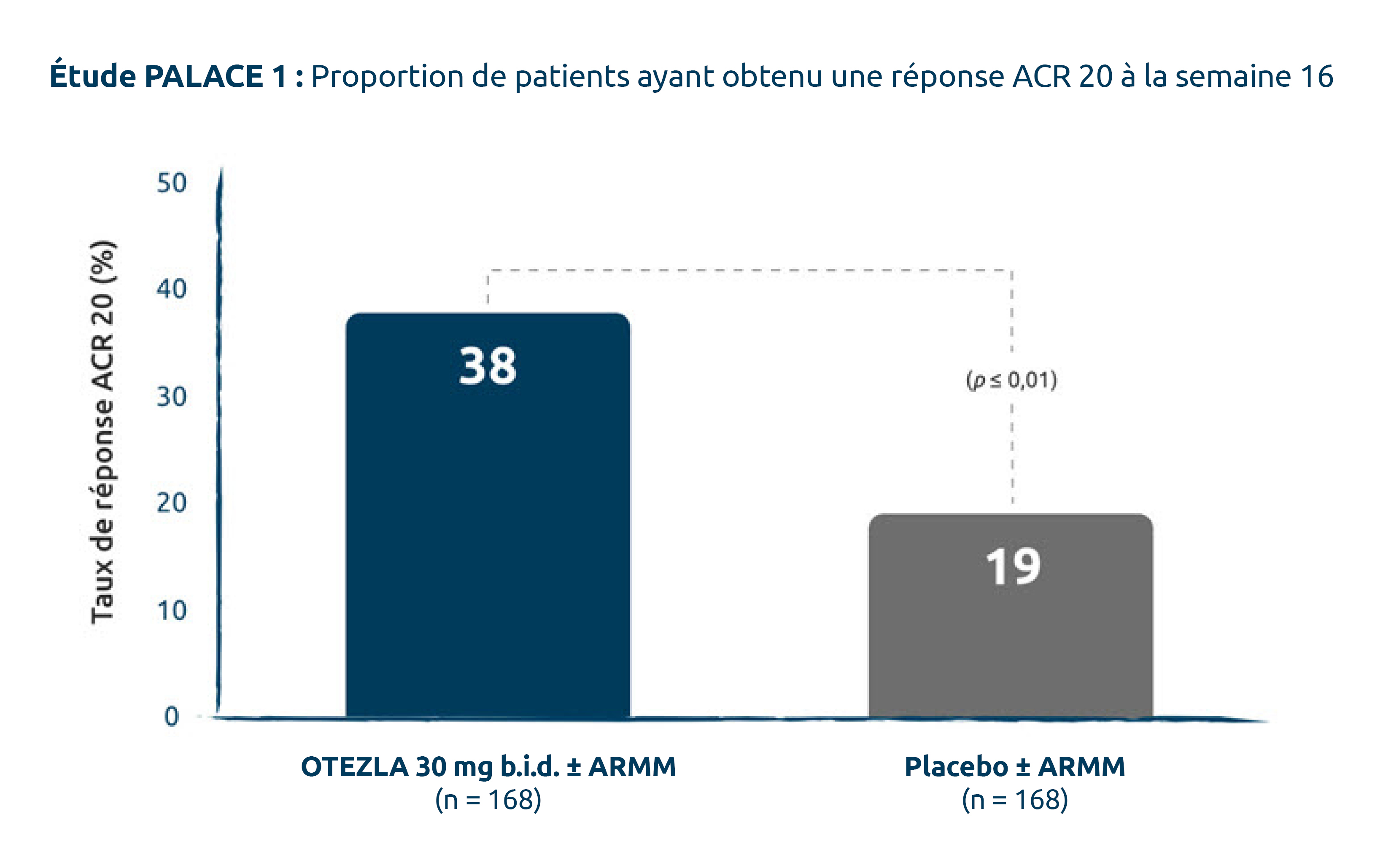
Population en intention de traiter; imputation des non-répondeurs.
D’après la monographie d’OTEZLA, 2020, et Kavanaugh A, et al., 20141,9.
Dans l'ensemble, les proportions plus élevées de patients ayant obtenu une réponse ACR 20 n'ont pas semblé être principalement dues à des améliorations moyennes d'un élément spécifique du score ACR (c.-à-d., nombre d'articulations sensibles, nombre d'articulations enflées, évaluation de la douleur par le patient, évaluation globale de la maladie par le patient, évaluation globale de la maladie par le médecin, score HAQ-DI et protéine C réactive)1.
RÉPONSE ACR 20 À LA SEMAINE 52 : AUCUN SIGNE D’ATTÉNUATION DE L’EFFICACITÉ, D’APRÈS LE TAUX DE RÉPONSE ACR 20, N’A ÉTÉ OBSERVÉ JUSQU’À LA SEMAINE 52 AVEC LE TRAITEMENT PAR OTEZLA (PHASE NON CONTRÔLÉE PAR PLACEBO DE L’ÉTUDE : SEMAINES 24 À 52)1,8
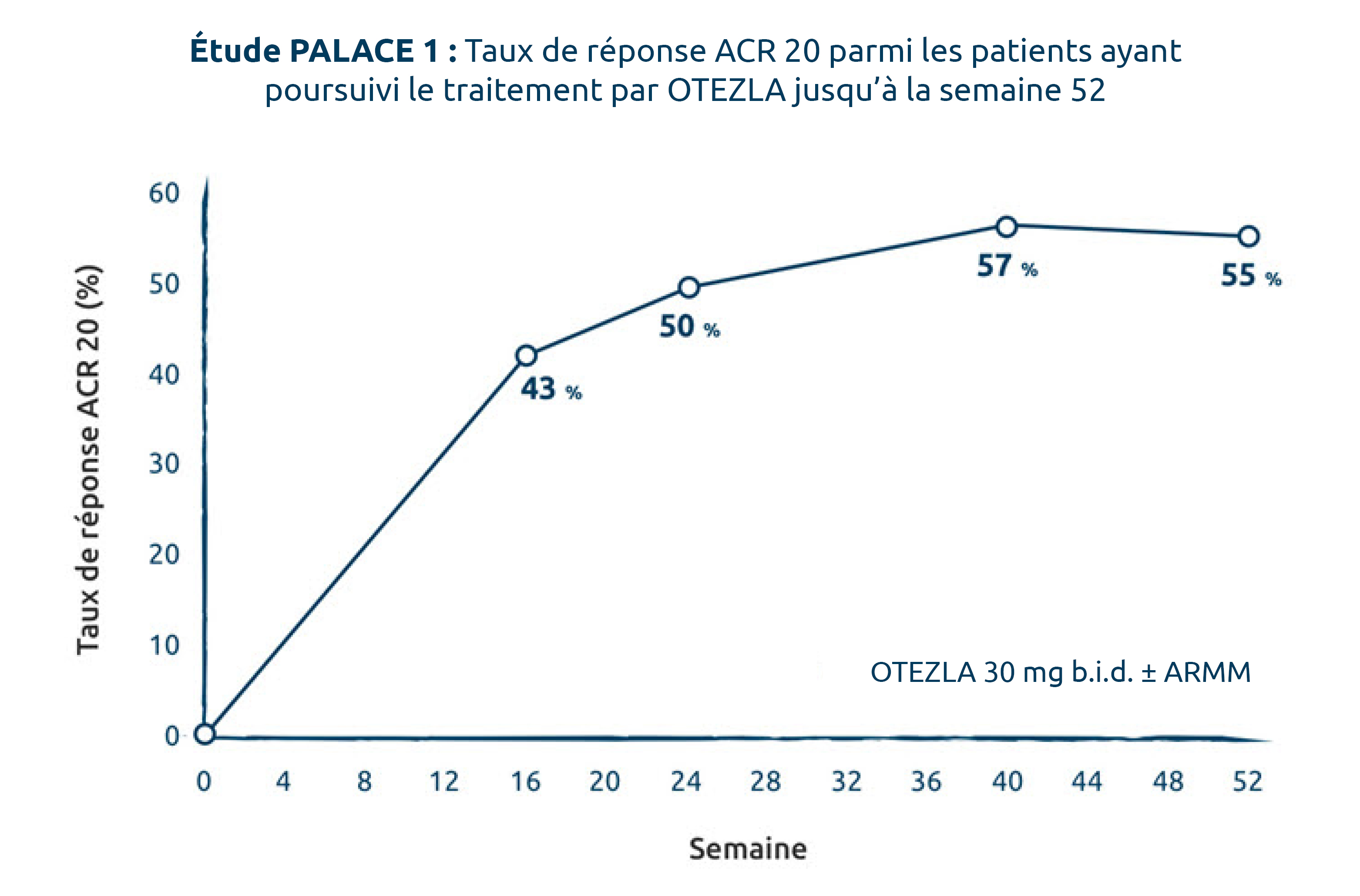
| Semaine de l’étude | 16 | 24 | 40 | 52 |
|---|---|---|---|---|
| OTEZLA 30 mg b.i.d. ± ARMM, n/m | 64/150 | 73/145 | 80/140 | 71/130 |
Patients recevant OTEZLA à 30 mg b.i.d. depuis le début de l’étude. Les données représentent les cas observés.
D’après la monographie d’OTEZLA, 2020, et Kavanaugh A, et al., 20151,8.

ACR : American College of Rheumatology; ARMM : antirhumatismal modifiant la maladie; b.i.d. : deux fois par jour; HAQ-DI : Health Assessment Questionnaire-Disability Index (indice d’invalidité selon le questionnaire d’évaluation de l’état de santé).